东京农业技术大学的研究人员报告了一项关于牙龈疾病(牙周炎)中骨质流失机制的新发现。他们发现双链RNA分子可以激活导致骨骼退化的免疫系统反应。
他们的论文发表在3月份的《生物化学杂志》上。
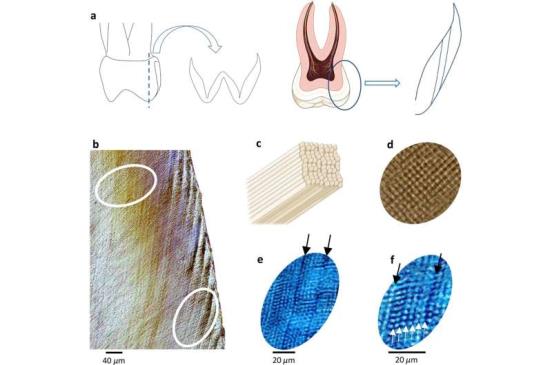
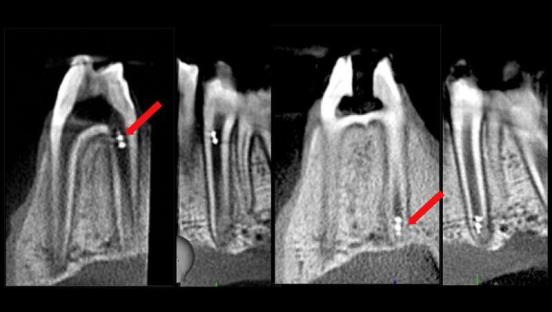
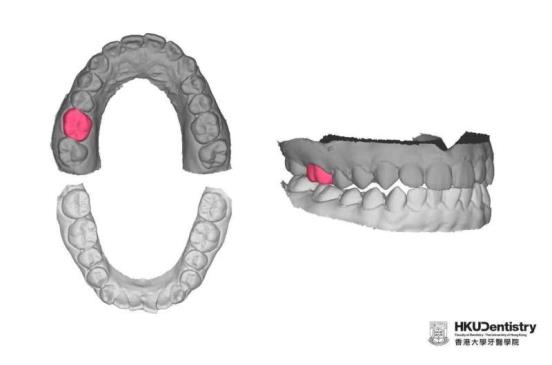
严重的牙龈感染会损害口腔软组织,比如牙龈,并逐渐侵蚀支撑牙齿的底层(牙槽骨)。牙齿底部周围的骨袋和将牙齿固定在颚骨上的韧带都很容易受到细菌感染的破坏。这种牙周骨侵蚀,如果不加以控制,最终可能导致牙齿脱落。
长期以来,人们一直认为,潜伏在牙槽内的菌斑是导致牙周病的原因。导致牙龈疾病的细菌外层膜的主要成分是一种叫做脂多糖的分子。脂多糖支持细菌细胞并保护其免受免疫细胞的攻击,但它也与牙龈炎症有关,因为它会打开免疫细胞上的toll样受体(TLR4),然后将细菌识别为病原体。
然而,到目前为止,还不清楚“其他病原体,包括来自细菌或自体细胞的双链RNA (dsRNA),是否有助于牙周骨丢失的进展,”该研究的作者、生物技术和生命科学系博士、博士稻田雅树教授解释说。例如,炎症组织中积累的中性粒细胞等免疫细胞可以在口腔中释放dsRNA。最近的研究怀疑dsRNA与牙周病期间的骨炎症进展有关。
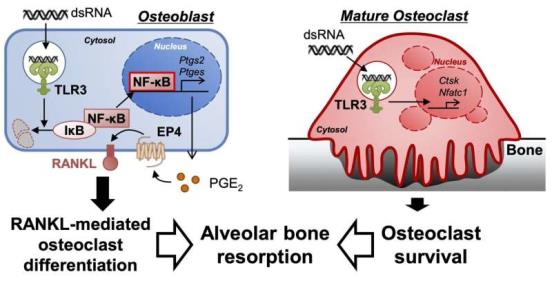
在健康的骨骼中,骨骼外表面的基质成骨细胞形成新的骨材料,而造血细胞产生的破骨细胞分解旧骨以吸收矿物质;它们活动之间的平衡维持着骨量。一种叫做RANKL的蛋白质在维持这种平衡中起着作用,因此,在骨骼如何成功重塑中起着作用。激素样PGE2(前列腺素E2)分子,由成骨细胞自然产生,在牙龈炎症期间上调RANKL。PGE2和RANKL生成的改变会影响骨丢失和增加。
研究人员使用小鼠的成骨细胞和骨髓细胞,加上一种类似于dsRNA的合成分子,对细胞暴露于dsRNA进行了实验。他们观察到,dsRNA明显诱导了更多破骨细胞的分化,破骨细胞是分解骨骼的细胞。dsRNA导致成骨细胞产生更多的激素样PGE2, PGE2反过来上调RANKL,刺激破骨细胞分化。因此,成骨细胞,通过与dsRNA分子的相互作用,发送细胞信号,增加侵蚀骨的破骨细胞的产生。dsRNA也使成熟破骨细胞存活更长时间。
更重要的是,存活时间较长的破骨细胞导致牙龈因细菌性疾病而发炎时对骨骼的吸附更多。这项研究揭示了一种以前未知的机制,即牙龈疾病导致骨骼分解。Inada说:“这些数据表明,基质成骨细胞中的TLR3信号控制PGE2的产生,并诱导随后成熟破骨细胞的分化和存活。”基质破骨细胞导致固定牙齿的骨炎性吸收。在牙周炎中导致骨骼损伤的炎症,可以由通过细菌或组织中积累的免疫细胞引入的dsRNA引发,这是对抗牙龈疾病影响的一个飞跃。
展望未来,研究人员计划进一步研究dsrna -通过向基质成骨细胞的免疫系统受体发出信号,以产生更多的pge2,如何促进牙周炎的发展。了解其潜在机制是开发新药物以防止牙龈疾病引起的骨质流失的基础。